Nous expliquons ce qu’est la conductivité électrique et en fonction de ce qu’elle varie. Conduction électrique des métaux, de l’eau et du sol.

Qu’est-ce que la conductivité électrique ?
La conductivité électrique est la capacité de la matière à laisser passer le courant électrique à travers ses particules . Cette capacité dépend directement de la structure atomique et moléculaire du matériau, ainsi que d’autres facteurs physiques tels que la température à laquelle il se trouve ou l’état dans lequel il se trouve ( liquide , solide , gaz ).
La conductivité électrique est l’opposé de la résistivité , c’est-à-dire la résistance des matériaux au passage de l’électricité . Il y a alors de bons matériaux et de mauvais conducteurs électriques, dans la mesure où ils sont plus ou moins résistants.
Le symbole pour représenter la conductivité est la lettre grecque sigma ( σ ) et son unité de mesure est le siemens par mètre (S/m) ou -1 ⋅ m -1 . Pour son calcul, les notions de champ électrique (E) et de densité de courant de conduction (J) sont généralement prises en compte , comme suit :
J = σE, d’où : σ = J/E
La conductivité varie selon l’ état de la matière . Dans les milieux liquides, par exemple, cela dépendra de la présence de sels dissous dans ceux-ci qui génèrent des ions chargés positivement ou négativement , et ce sont les électrolytes chargés de conduire le courant électrique lorsque le liquide est soumis à un champ électrique.
Par contre, les solides présentent une structure atomique beaucoup plus fermée et avec moins de mouvement , donc la conductivité va dépendre du nuage d’ électrons partagé par les bandes de valence et la bande de conduction, qui varie selon la nature atomique de la matière : la Les métaux sont de bons conducteurs électriques et les non-métaux , en revanche, sont de bonnes résistances (ou isolants, comme le plastique ).
Voir aussi: Conductivité thermique
conductivité de l’eau
L’eau est généralement un bon conducteur électrique. Cependant, ladite capacité dépend de sa marge de solides dissous totaux (TDS) , car la présence de sels et de minéraux dans l’eau forme les ions électrolytiques qui permettent le passage du courant électrique. La preuve en est que l’eau distillée , dont tous les ions dissous sont éliminés (par distillation et autres méthodes), et ne conduit pas l’électricité.
De cette façon, la conductivité de l’eau salée est supérieure à celle de l’eau douce . L’augmentation du taux de conductivité peut être enregistrée au fur et à mesure que des ions dissous dans le liquide sont ajoutés, jusqu’à atteindre une limite de concentration ionique dans laquelle des paires d’ions se forment, positives avec négatives, qui annulent leur charge et empêchent la conductivité d’augmenter. augmenté davantage.
conductivité du sol

Les sols , en général, ont une conductivité électrique différente, en fonction de divers facteurs tels que l’irrigation de l’eau ou la quantité de sels qu’ils contiennent. Tout comme dans le cas de l’eau, les sols plus salins seront de meilleurs conducteurs électriques que les sols moins salins , et cette distinction est souvent déterminée par la quantité d’eau qu’ils reçoivent (puisque l’eau peut « laver » les sels du sol).
Ce niveau de salinité est souvent confondu avec la sodicité du sol (la présence de sodium), alors qu’en fait la salinité fait référence à l’abondance des cations sodium (Na + ), potassium (K + ), calcium (Ca 2 + ) et magnésium (Mg 2+ ), ainsi que les cations de chlore (Cl – ), sulfate (SO 4 2- ), bicarbonate (HCO 3 – ) et carbonate (CO 3 2- ).
Ainsi, dans de nombreux cas, des techniques telles que le lavage (pour les sols très salins) ou l’injection d’autres éléments neutralisants (comme le soufre) pour les sols très basiques sont utilisées. Cela peut souvent être déterminé en effectuant des tests électriques.
conductivité des métaux
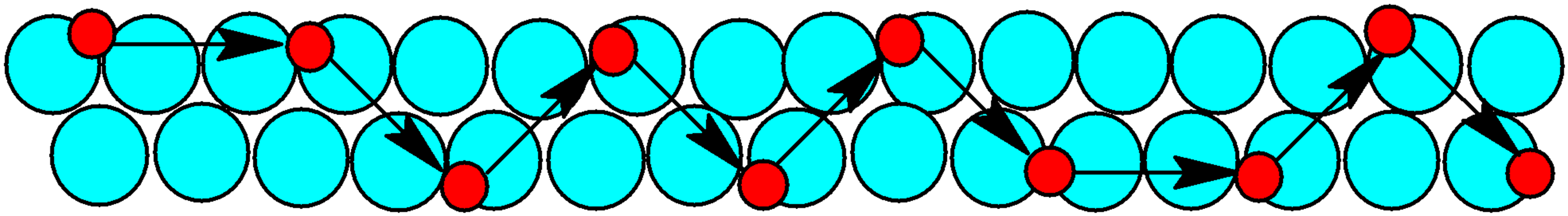
Les métaux sont généralement d’excellents conducteurs électriques . En effet, les atomes de ce type de matériau se combinent en formant des liaisons métalliques . Dans les métaux, les électrons restent autour du métal comme un nuage, se déplaçant autour des noyaux atomiques étroitement liés, et ce sont eux qui permettent le flux électrique.
Lors de l’application du métal à un champ électrique, les électrons circulent librement d’une extrémité du métal à l’autre, tout comme cela se produit également avec la chaleur , dont ils sont tous deux de bons émetteurs. C’est pourquoi le cuivre et d’autres métaux sont utilisés dans le câblage électrique et les appareils électroniques. La figure suivante représente schématiquement le flux d’ électrons (en rouge) lorsqu’un champ électrique est appliqué à un métal :