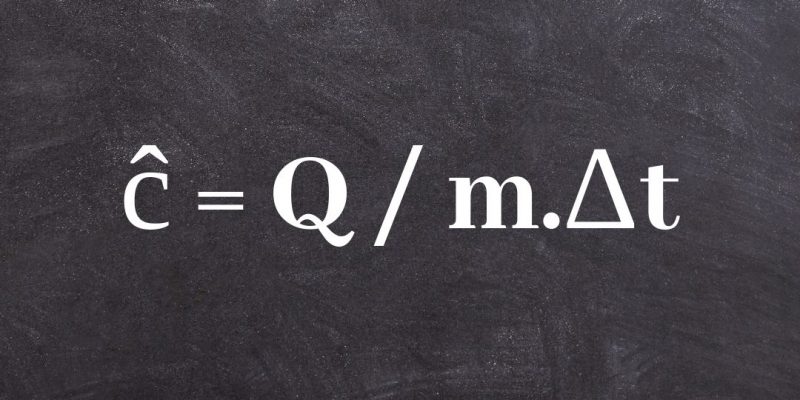Nous expliquons ce qu’est l’équilibre thermique, en quoi il consiste et quelle est sa formule. En outre, la loi zéro de la thermodynamique et des exemples.
Qu’est-ce que l’équilibre thermique ?
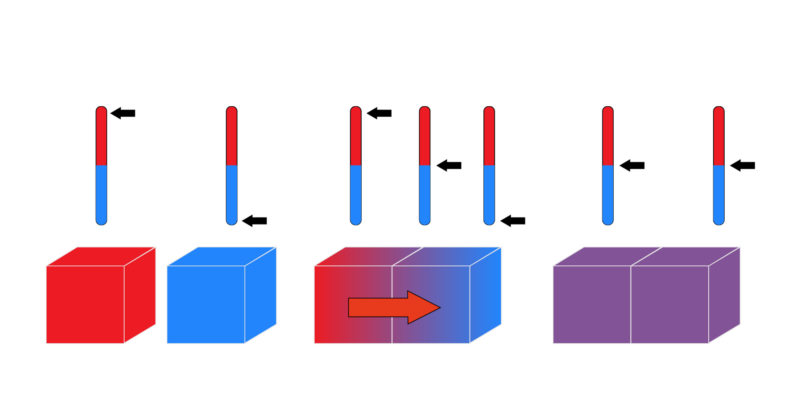
En physique , l’ équilibre thermique est appelé l’état dans lequel deux corps en contact, ou séparés par une surface conductrice, égalisent leurs températures initialement disparates, en raison du transfert de chaleur de l’un à l’autre.
Si nous avons deux objets en contact, l’un plus chaud que l’autre, au fil du temps, les deux auront tendance à atteindre la même température et, s’il n’y a pas de transfert de chaleur vers d’autres objets, ils maintiendront désormais un équilibre thermique, c’est-à-dire , une constante de température .
Il peut vous aider : Conductivité thermique
Qu’est-ce que l’équilibre thermique ?

Ce phénomène peut être expliqué au microscope, en comprenant que la température des objets est directement liée à l’ énergie cinétique moyenne de leurs particules , qu’il s’agisse d’ atomes , de molécules ou de tout ce qu’il convient de considérer. Cette moyenne est ce que l’on appelle communément « l’énergie interne » en physique, de sorte que plus l’énergie cinétique est élevée, plus l’énergie interne est élevée et plus la température du système est élevée .
Deux corps en contact échangent de l’énergie au fil du temps . Ainsi, le point d’équilibre thermique est atteint lorsque l’énergie cinétique des deux corps est égale, de sorte que les deux corps commencent à fonctionner comme un seul système thermodynamique, doté de la même quantité d’énergie interne et, par conséquent, de température.
Formule d’équilibre thermique
L’expression de l’équilibre thermique implique le calcul de la différence de température entre les deux corps, il faut donc déterminer la quantité de chaleur (Q) qu’ils échangent.
Ceci est déterminé à l’aide de la formule Q = m. Ce. Δt , où m sera la masse du corps, Ce sa chaleur spécifique exprimée en cal / gr °C, et Δt la variation de température, soit : Δt = tf – ti, temps final moins temps initial.
Une fois la chaleur Q pour chaque corps calculée, nous pourrons les comparer sachant que l’équilibre thermique se produit dans l’égalité des températures entre le corps 1 et le corps 2. Pour atteindre l’équilibre thermique, la chaleur que gagne le corps le plus froid est la celle que le corps le plus chaud perd , donc Q1 = Q2, c’est-à-dire chaleur gagnée = chaleur perdue.
Loi zéro de la thermodynamique
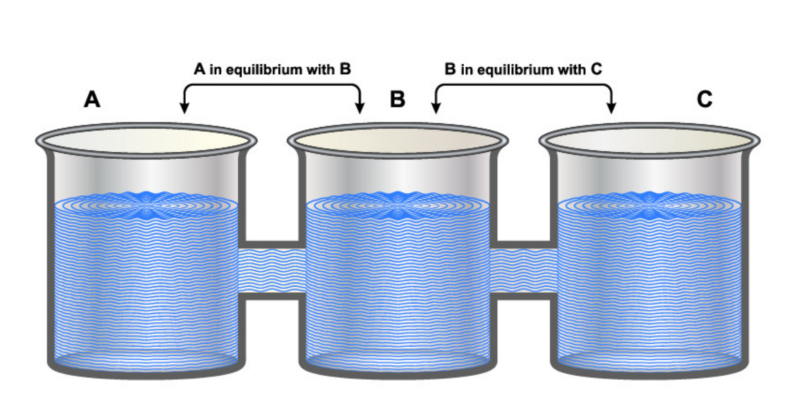
Ce principe est exprimé dans la soi-disant loi zéro de la thermodynamique, qui a été exprimée en 1931 par RH Fowler comme suit : « Si deux systèmes A et B sont, chacun séparément, en équilibre thermique avec un troisième système , que nous appellerons C , alors A et B sont également en équilibre thermique l’un avec l’autre.
Autrement dit : si A = C et B = C, alors A = B.
Grâce à ce principe, centré sur la formulation mathématique de la thermodynamique, on sait ce que Maxwell exprimait ainsi en mots : « Toute chaleur est du même type » .
Exemples d’équilibre thermique
Voici quelques exemples simples d’équilibre thermique :
- Lorsque nous entrons dans une pièce chaude, nous percevons immédiatement la chaleur de l’ air mais étant donné un laps de temps , notre corps échangera de la chaleur avec l’air et entrera en équilibre thermique avec lui, nous cesserons donc de percevoir la différence de température.
- Si nous introduisons un récipient en verre avec de l’eau froide à l’intérieur d’un récipient plus grand avec de l’eau bouillante, le flux de chaleur entre les deux refroidira l’eau chaude et réchauffera l’eau froide, jusqu’à atteindre un niveau d’équilibre thermique intermédiaire.
- Les produits que nous avons dans notre congélateur de cuisine sont en équilibre thermique par rapport à l’air congelé entre eux, de sorte qu’ils partagent tous la même température.