Nous expliquons quelles sont les méthodes de séparation des mélanges et nous définissons chacune de ces méthodes avec quelques exemples simples.

Quelles sont les méthodes de séparation des mélanges ?
Les méthodes de séparation des mélanges ou les méthodes de séparation des phases sont connues comme les différentes procédures physiques qui permettent de séparer deux ou plusieurs composants d’un mélange . Les composants du mélange conservent leur identité et leurs propriétés chimiques après séparation.
Pour que ces mécanismes fonctionnent, il faut qu’il s’agisse de mélanges dans lesquels les composants conservent leur identité et qu’il n’y ait pas eu de réactions chimiques altérant durablement leurs propriétés ou donnant naissance à de nouvelles substances.
Pour que les méthodes de séparation soient applicables, des propriétés telles que le point d’ébullition , la densité ou la taille doivent être préservées dans les composants du mélange.
En revanche, ces méthodes fonctionnent aussi bien en mélanges homogènes qu’en mélanges hétérogènes , puisqu’elles n’impliquent aucune modification de l’identité des composants, qui peuvent ainsi être récupérés plus ou moins tels qu’ils étaient avant mélange. Selon la méthode appliquée, les composants d’origine seront obtenus avec une pureté plus ou moins grande.
Voir aussi: États d’agrégation de la matière
décantation
La décantation est une méthode utilisée pour séparer les liquides qui ne se dissolvent pas les uns dans les autres (comme l’eau et l’huile) ou les solides insolubles dans un liquide (comme l’eau et le sable).
Il consiste en l’utilisation d’une ampoule ou d’une ampoule à décanter , où le mélange est laissé au repos jusqu’à ce que l’ingrédient le plus dense se dépose et coule au fond. La valve est ouverte et elle est relâchée, en la fermant à temps pour que l’ingrédient le moins dense reste à l’intérieur. Cette méthode est souvent utilisée comme première étape vers l’obtention de substances plus pures.
Continuer sur : Décantation
Filtration
La filtration est une méthode utile pour séparer les solides insolubles des liquides . Elle consiste en l’utilisation d’un filtre (papier filtre, pierres filtrantes, etc.) qui permet le passage du liquide à travers un milieu poreux et retient les éléments solides.
C’est ainsi que fonctionnent les filtres à eau de nos maisons , ou le papier filtre où l’on verse le café solide avant d’ajouter l’eau chaude. L’eau (qui contient les particules de café les plus fines) passe à travers le papier et les particules de café les plus grossières y sont retenues.
Continuer sur : Filtration
séparation magnétique
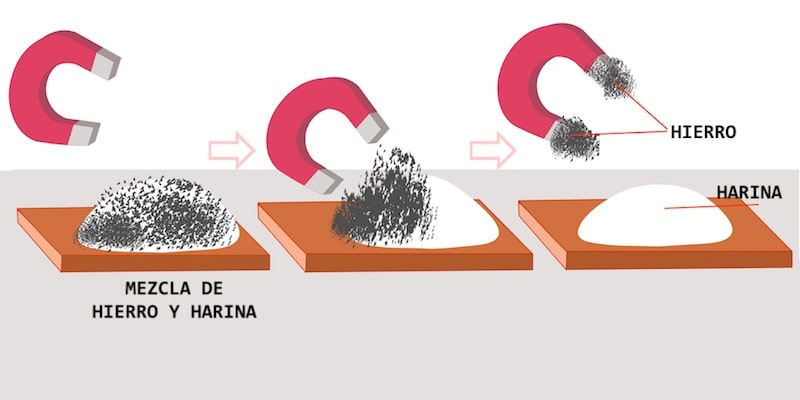
La séparation magnétique consiste en la séparation des phases selon leur potentiel magnétique . Certaines substances réagissent aux champs magnétiques et d’autres non, et selon cette différence, un aimant ou un électroaimant est appliqué au mélange, ce qui permet d’attirer un composant et de laisser l’autre intact (par exemple, des fragments de fer dans le sol, mercure dans l’eau). , morceaux de métal dans l’eau).
Continuer sur : Séparation magnétique
tamisage

Le tamisage fonctionne de la même manière que le filtrage, mais entre des substances solides de différentes tailles (comme le gravier et le sable, le sel et le pop-corn, ou le riz et les cailloux).
Un filet ou tamis est utilisé, dont les trous permettent le passage des plus petits fragments et retiennent les plus gros. Selon le matériau, il peut être utilisé comme première étape pour obtenir des substances pures ou comme étape finale.
Continuer sur : Tamisage
Distillation
La distillation permet de séparer des liquides solubles les uns dans les autres , mais ayant des points d’ébullition différents (comme l’eau et l’alcool ). La différence entre les points d’ébullition des composants à séparer par cette méthode doit être d’environ 80 ºC.
La procédure consiste à verser le mélange dans un récipient et à le chauffer, en contrôlant la température de manière à ce que seul le composant ayant le point d’ébullition le plus bas s’évapore, et soit acheminé par un conduit (appelé colonne de distillation) vers un autre récipient, cette fois réfrigéré. . Là, il se condensera et reviendra à sa phase d’origine.
Les liquides ainsi obtenus sont appelés distillats (eau distillée, alcool distillé).
Suivi : Distillation
Cristallisation
La cristallisation est une méthode idéale pour séparer les solides dissous dans les liquides (sel dans l’eau, sucre dans l’eau). Elle consiste à évaporer le liquide jusqu’à obtenir les cristaux du solide dissous au fond du récipient. Par exemple, c’est ainsi que le sel de mer est obtenu. Selon le taux d’ évaporation , les cristaux seront plus gros ou plus petits.
Continuer sur : Cristallisation
Flottation

La flottation est l’opposé de la décantation et consiste à laisser flotter la phase solide de plus faible densité dans le liquide puis à l’éliminer manuellement ou à travers un tamis. L’exemple parfait en est la procédure de nettoyage de la piscine.
Chromatographie
La chromatographie est une méthode utilisée pour séparer des mélanges complexes qui ne répondent à aucune autre méthode de séparation . Elle utilise la capillarité comme principe : processus qui permet l’avancée d’une substance à travers un milieu spécifique. Les deux phases du mélange sont ainsi identifiées comme phase mobile (celle qui avance) et phase stationnaire (sur laquelle elle avance).
Le fonctionnement de cette séparation dépend de l’affinité des composants du mélange pour les deux phases, et selon cette affinité, la séparation sera plus ou moins rapide. Par exemple, lorsqu’on renverse du café sur un chiffon, le café avance en occupant une grande surface.
Il existe actuellement différentes méthodes de chromatographie :
- Chromatographie papier . La phase stationnaire est constituée d’une bande de papier filtre et la phase mobile est constituée d’un solvant contenant l’échantillon à séparer. Quelques gouttes du solvant contenant l’échantillon sont placées sur une extrémité du papier et on laisse le liquide avancer. Ensuite, on laisse sécher, et si les différents composants de l’échantillon ont des couleurs différentes, on peut observer leurs différentes positions sur le papier.
- Chromatographie sur couche mince. La phase stationnaire est composée d’un matériau absorbant collé sur une plaque qui peut être en verre, en aluminium ou autre matériau. La phase mobile est un liquide qui va jouer le rôle d’éluant. La procédure consiste à déposer l’échantillon sur la plaque puis à en immerger une partie dans l’éluant. Les composants seront séparés par différence d’affinité entre l’éluant et le composant collé à la plaque.
- chromatographie sur colonne. La phase stationnaire consiste en un matériau absorbant solide qui est conditionné dans une colonne en verre (bien que des colonnes en d’autres matériaux, par exemple en acier inoxydable, existent aujourd’hui). La phase mobile est constituée d’un éluant et la séparation des composants de l’échantillon dépend de l’affinité que ses composants ont pour les deux phases. Habituellement, l’éluant traverse la colonne par gravité , bien que des méthodes modernes aient été développées où il est entraîné par des pompes qui appliquent une pression .
Continuer sur : Chromatographie