Nous expliquons ce que sont les non-métaux et quelques exemples de ces éléments chimiques. Aussi, leurs propriétés et ce que sont les métaux.

Que sont les non-métaux ?
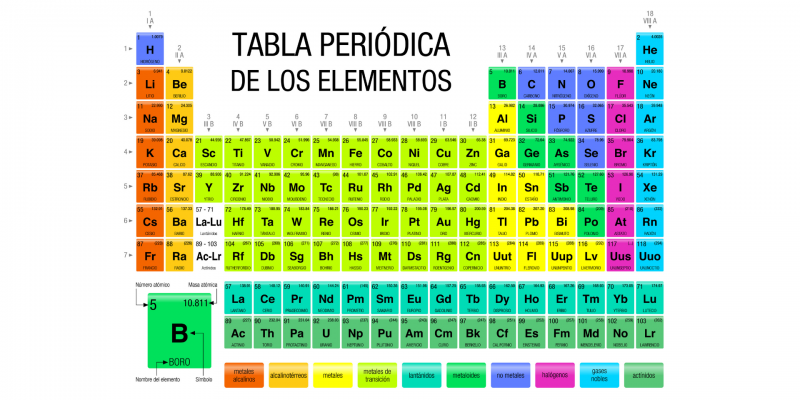
Les non-métaux sont des éléments rares dans le tableau périodique et se caractérisent par le fait qu’ils ne sont pas de bons conducteurs de chaleur ou d’électricité . Ses propriétés sont très différentes de celles des métaux . D’autre part, ils forment des liaisons covalentes pour former des molécules entre eux.
Les éléments essentiels à la vie font partie des non-métaux (oxygène, carbone, hydrogène, azote, phosphore et soufre). Ces éléments non métalliques ont des propriétés et des aspects très divers : ils peuvent être solides , liquides ou gazeux à température ambiante .
Voir aussi: Composé inorganique
exemples de non-métaux

Ils sont principalement classés comme suit :
- Halogènes. Fluor (F), chlore (Cl), brome (Br), iode (I), astatine (At) et tension (Ts).
- gaz nobles . Hélium (He), néon (Ne), argon (Ar), krypton (Kr), xénon (Xe), radon (Rn), oganesson (Og).
- Autres non-métaux. Hydrogène (H), carbone (C), soufre (S), sélénium (Se), azote (N), oxygène (O), sélénium (Se) et phosphore (P).
Propriétés des non-métaux

Les non-métaux se distinguent des métaux en ce que :
- Ils ne sont généralement pas de bons conducteurs, ni de la chaleur ni de l’électricité.
- Ils présentent différents états d’agrégation dans les conditions normales : solide (comme le soufre), gazeux (comme l’hydrogène) ou liquide (comme le brome).
- Ils ont des points de fusion très bas (par rapport aux métaux).
- Ils ne sont pas brillants et ont généralement des couleurs différentes .
- Ils ne sont ni ductiles ni malléables.
- Ils acquièrent toujours une charge négative lorsqu’ils sont ionisés.
- Lorsqu’ils sont combinés avec de l’oxygène, ils forment des anhydrides (oxydes non métalliques).
- Ils ont dans leur dernière couche (couche de valence) 4, 5, 6, 7 ou 8 électrons .
- Ils forment principalement des molécules de deux ou plusieurs atomes .
métaux

Les métaux ou métaux sont des éléments du tableau périodique qui se caractérisent par être de bons conducteurs d’électricité et de chaleur . Ce sont des éléments à haute densité et qui, en général, sont solides à température ambiante (sauf le mercure). De plus, leur capacité à réfléchir la lumière leur confère un éclat caractéristique.
Les métaux sont les éléments les plus nombreux du tableau périodique et certains sont parmi les plus abondants de la croûte terrestre .
Les métaux présentent des « liaisons métalliques ». Dans les liaisons métalliques, les atomes métalliques sont situés à proximité les uns des autres et sont tous « immergés » dans leurs électrons de valence , formant la structure métallique. Cela se produit parce que les atomes métalliques sont unis de telle manière que leurs noyaux atomiques se rejoignent avec les électrons de valence (électrons situés dans la dernière couche électronique), qui forment une sorte de nuage autour d’eux.
Plus dans: Métaux