Nous expliquons ce qu’est la séparation magnétique, ses caractéristiques, des exemples et d’autres techniques de séparation de mélange.
Qu’est-ce que la séparation magnétique ?
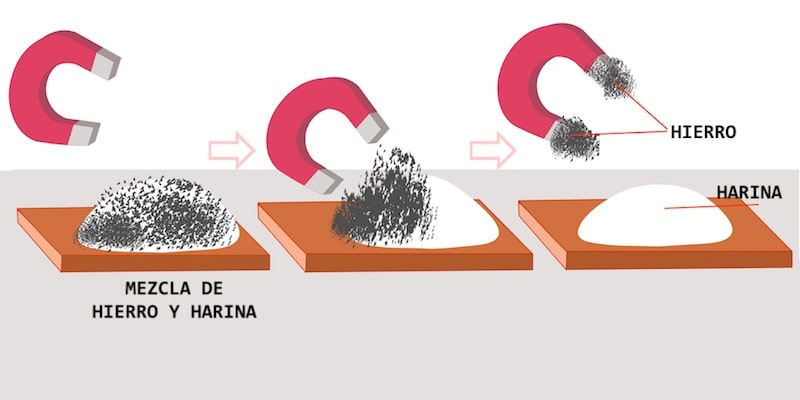
La séparation magnétique est une méthode physique de séparation des mélanges , qui utilise la susceptibilité magnétique de certains de ses composants. Pour ce faire, il recourt à exposer le mélange à un aimant (ou à un champ magnétique suffisamment intense ) pendant un certain temps.
En d’autres termes, la technique consiste à rapprocher un aimant du mélange, pour attirer les composants ferromagnétiques du mélange, laissant les non magnétiques dans le récipient.
Le magnétisme se manifeste par une force d’attraction ou de répulsion , selon la polarité des champs magnétiques opposés : des pôles égaux se repoussent, des pôles différents s’attirent . C’est une propriété de la matière qui est présente dans toute matière et qui est plus perceptible dans certains matériaux que dans d’autres.
La technique de séparation magnétique est largement utilisée dans les tâches de recyclage ou de récupération de certains éléments métalliques , qui diffèrent de leur environnement par leur nature moléculaire. Il existe même des variantes applicables aux substances organiques polaires, mais ce sont des procédés plus délicats.
Il peut vous aider : Méthodes de séparation des mélanges
Caractéristiques de la séparation magnétique

La séparation magnétique fonctionne sur la base de l’énorme différence de susceptibilité magnétique qui peut exister entre les composants d’un mélange. Tous ceux qui réagissent au magnétisme subiront des modifications lorsqu’ils seront exposés à un aimant ou à un électroaimant, laissant les autres à leur place.
Évidemment, idéalement, tous les composants du mélange ne sont pas magnétiques ou pas tous dans la même mesure, de sorte que grâce à une exposition contrôlée aux forces magnétiques, le mélange peut être efficacement séparé.
Exemples de séparation magnétique
Cette technique est très utile pour séparer des mélanges tels que :
- Limaille de fer présente dans la farine, le soufre, le gravier ou d’autres matériaux solides .
- Pièces de monnaie , clips, objets métalliques du sable sur la plage.
- Nickel massif parmi d’autres métaux moins magnétiques, comme le bronze ou l’argent.
Autres méthodes de séparation des mélanges

En plus de la séparation magnétique, il existe d’autres méthodes physiques et chimiques pour séparer les mélanges, telles que :
- Filtré . Utile pour séparer les solides non solubles des liquides , il consiste en l’utilisation d’un filtre (papier filtre, pierres filtrantes, etc.) qui permet le passage du liquide mais retient les éléments solides.
- Décantation . Utilisé pour séparer les liquides qui ne se dissolvent pas les uns dans les autres, ou les solides insolubles dans un liquide, à l’aide d’une ampoule ou d’une ampoule à décanter, où le mélange est laissé reposer jusqu’à ce que le composant le plus dense coule au fond, tandis que le moins dense reste sur le surface.
- Tamisé . C’est une méthode de séparation similaire au filtrage, mais elle est utilisée pour séparer des mélanges de substances solides de différentes tailles. Elle se fait à l’aide d’un filet ou d’un tamis, dont les trous permettent le passage des plus petits fragments et retiennent les plus gros.
- Distillation . Il permet de séparer les liquides solubles les uns des autres, qui ont des points d’ébullition différents . La procédure consiste à verser le mélange dans un récipient et à le chauffer, en contrôlant la température afin que seul le composant ayant le point d’ébullition le plus bas se vaporise et puisse être redirigé vers un autre récipient, où il se condense.
- Évaporation . Il est utilisé pour séparer les solides dissous dans les liquides et consiste à évaporer le liquide jusqu’à l’obtention des cristaux du solide dissous au fond du récipient.
Continuer avec : Solution chimique