Nous expliquons ce qu’est la matière en physique et quelles sont ses caractéristiques. De plus, les états qu’il présente et sa structure.

Qu’est-ce que la matière (physique) ?
Selon l’ approche physique , la matière désigne toute entité dotée d’ une masse propre et capable d’occuper l’espace à un instant donné. Tous les objets physiques sont composés de matière, d’une voiture à un atome et les particules élémentaires qui le composent.
La notion de matière dans le domaine de la physique a été définie et redéfinie au cours des siècles, depuis les temps anciens (lorsque la notion d’atome a émergé), jusqu’à l’époque d’Isaac Newton puis d’Albert Einstein. La découverte de la matière subatomique et l’inauguration de la physique des particules ont été l’événement le plus révolutionnaire dans le domaine de la réflexion sur la matière.
Ainsi, la définition initiale de la matière que nous avons donnée était suffisante pour les branches classiques de la physique, mais elle est problématique dans le domaine de la mécanique quantique , où les notions de « masse » et « d’espace » sont beaucoup plus compliquées.
Voir aussi: Propriétés générales de la matière
Caractéristiques de la matière en physique

La matière a certaines propriétés spécifiques, telles que la masse et le volume , c’est-à-dire que la matière occupe une certaine région de l’espace-temps. Cela signifie que la matière a des propriétés mesurables, telles que les proportions ( longueur , largeur, hauteur) , la densité , le poids , la dureté, la fluidité, la malléabilité, entre autres. Connaître la matière, c’est comprendre précisément ses propriétés physiques, radicalement différentes de celles, par exemple, de l’énergie .
D’autre part, la matière doit être dans l’un des états ou phases connus , selon la distribution, le groupement et les propriétés de ses particules . Ainsi, la matière existe à l’état solide , liquide et gazeux , bien qu’elle puisse également se trouver à l’état de plasma (gaz ionisé) dans certaines conditions extrêmes de pression et de température. Il existe d’autres états plus complexes de la matière qui sont étudiés dans des domaines avancés de la physique et qui sont instables.
En plus de la matière, il existe de l’antimatière , qui peut être comprise comme une matière constituée d’antiparticules. Pour chaque particule élémentaire qui existe, il en existe une autre identique mais de charge électrique opposée , qui provoque l’annihilation des deux lors de l’interaction.
États de la matière

Selon la physique, il existe trois états principaux de la matière : solide, liquide et gazeux, bien qu’il existe également d’autres états moins fréquents, comme le plasma ou les condensats fermioniques, reproductibles uniquement en laboratoire. Chaque état physique a des caractéristiques différentes qui ont beaucoup à voir avec la façon dont les particules du système étudié sont disposées dans l’espace et l’énergie dont elles disposent.
- solides . Les particules de matière solide sont très, très proches les unes des autres, en proie à des forces attractives très fortes. Pour cette raison, ils se comportent comme un seul corps, avec une grande cohésion, une densité et une forme constante. Ils résistent à la fragmentation et ont une fluidité faible ou nulle : ils ne peuvent pas être comprimés et, lorsqu’ils sont cassés ou fragmentés, d’autres solides plus petits en sont obtenus.
- Liquides . Les particules de matière liquide sont maintenues ensemble par des forces attractives, beaucoup plus faibles et moins ordonnées que celles des solides. Pour cette raison, les liquides manquent d’une forme fixe et stable, ainsi que de cohésion et de résistance , ils acquièrent donc la forme du récipient qui les contient. Ils ont une grande fluidité (ils peuvent tenir dans de petits espaces) et une tension superficielle qui les fait adhérer aux surfaces, ils sont peu compressibles et, à l’exception de l’eau , ils ont tendance à se contracter en présence de froid.
- Gaz . Les particules de matière gazeuse sont dans un tel état de dispersion et d’éloignement qu’elles parviennent à peine à rester ensemble : la force d’attraction entre elles est faible, ce qui provoque un état de désordre entre elles. Puisqu’ils ne peuvent pas se réunir et former un corps massif et compact, la gravité n’a aucun effet appréciable sur eux. Ils occupent un volume beaucoup plus important que les liquides et les solides, car ils ont tendance à se dilater jusqu’à occuper tout l’ espace qui les contient. Ils n’ont pas de forme et de volume fixes et sont parfois incolores et/ou inodores.
La matière ne peut passer d’un état à un autre qu’en modifiant les conditions de température et de pression dans lesquelles elle se trouve. Ses propriétés chimiques resteront cependant les mêmes.
Plus dans: États de la matière
structure de la matière

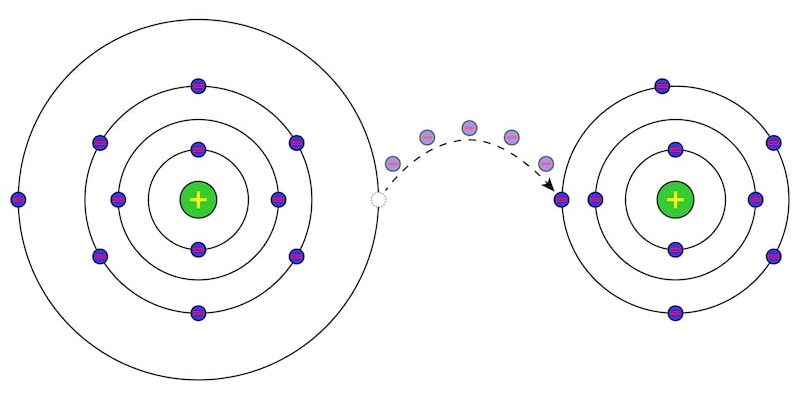
Toute matière connue est composée d’ unités microscopiques appelées atomes formées, à leur tour, par trois particules subatomiques :
- Électrons . Dotées d’une charge négative et de petite taille, ces particules orbitent autour du noyau de l’atome selon un ensemble de trajectoires appelées orbitales, avec une énergie plus ou moins importante selon leur proximité ou leur éloignement du noyau.
- protons . Dotés d’une charge positive et de taille plus importante, ils se trouvent dans le noyau de l’atome, et constituent l’essentiel de sa masse et de son poids.
- Neutrons . Sans aucune charge électrique, ils se trouvent dans le noyau de l’atome avec les protons, contribuant à la masse et au poids de l’atome bien qu’ils n’influencent pas son électromagnétisme .
Selon le nombre d’électrons, de protons et de neutrons qu’un atome possède, il se conformera aux éléments chimiques connus et classés dans le tableau périodique. Par exemple, l’atome le plus simple qui existe est l’hydrogène, qui n’a qu’un électron et un proton.