Nous expliquons ce que sont les protons, comment ils ont été découverts, leurs propriétés et caractéristiques. Aussi, que sont les nucléons.

Qu’est-ce qu’un proton ?
Le proton est un type de particule subatomique , c’est-à-dire l’une des plus petites particules qui composent l’atome. Il appartient à la famille des fermions et est doté d’ une charge électrique positive .
Toute matière est constituée d’ atomes , eux-mêmes composés essentiellement de trois types de particules dotées de charges électriques différentes : les électrons (charge négative), les neutrons (charge neutre) et les protons (charge positive).
Pendant longtemps, on a pensé que le proton était un type fondamental de particule, c’est-à-dire qu’il ne pouvait pas être divisé. Cependant, il existe maintenant des preuves solides qu’il est composé de quarks .
Dans tous les cas, le proton est une particule subatomique stable. Contrairement à l’électron, qui orbite autour du noyau de l’atome, les protons sont contenus dans le noyau atomique avec les neutrons , contribuant à la majeure partie de la masse atomique.
Voir aussi: Modèles atomiques
découverte du proton

Les protons ont été découverts en 1918 par Ernest Rutherford (1871-1937), chimiste et physicien britannique. Au milieu d’expériences avec de l’azote gazeux , Rutherford a remarqué que ses instruments détectaient la présence de noyaux d’hydrogène en projetant des particules alpha sur le gaz.
Il en conclut que ces noyaux doivent être des particules fondamentales de matière, sans savoir à l’époque que, justement, le noyau de l’atome d’hydrogène contient une seule particule : un proton. Ainsi, il a été décidé de donner à l’hydrogène le numéro atomique 1 .
Cependant, il est connu des expériences scientifiques précédentes qui ont conduit à cette découverte . Par exemple, le physicien allemand Eugene Goldstein (1850-1930) a trouvé en 1886 des ions positifs à l’intérieur de l’atome, grâce à des expériences avec des rayons cathodiques.
De plus, le britannique JJ Thompson (1856-1940) avait déjà découvert les électrons et leur charge négative, c’est-à-dire qu’il fallait qu’il y ait un autre type de particule de charge opposée dans l’atome.
Voir aussi: modèle atomique de Rutherford
Propriétés et caractéristiques du proton
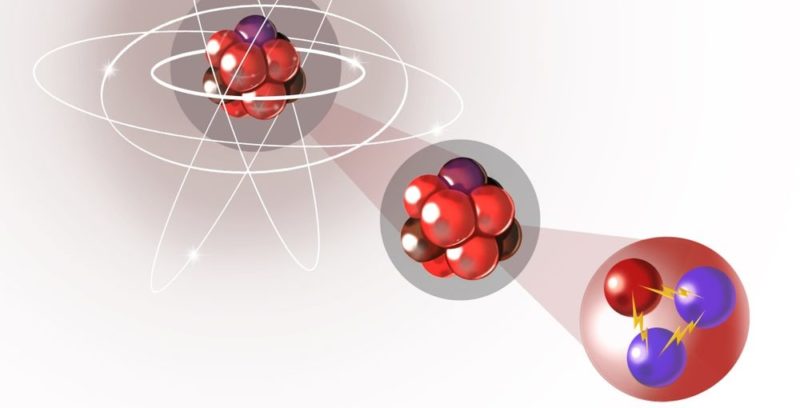
Les protons sont des particules composites stables , beaucoup plus massives qu’un électron (1836 fois) et dotées d’une charge élémentaire positive de 1 (1,6 x 10 -19 C). Ils sont composés de trois particules élémentaires ou quarks : deux « up » (up) et un « down » (down). Leur demi-vie est supérieure à 10 35 ans , après quoi ils sont susceptibles de se décomposer.
Comme les autres particules subatomiques, les protons ont leur propre spin, c’est-à-dire un moment cinétique intrinsèque et invariable, qui dans ce cas est de ½ . Cette propriété est particulièrement utile pour l’imagerie par résonance magnétique nucléaire et d’autres applications technologiques modernes.
nucléons
Puisqu’ils se trouvent normalement dans le noyau atomique, les protons et les neutrons sont appelés « nucléons » . Les électrons, quant à eux, gravitent autour d’eux de manière plus ou moins dispersée.
Les nucléons sont liés entre eux par les forces nucléaires fortes , qui seulement dans le cas d’atomes particulièrement gros (comme l’uranium) peuvent céder le pas à d’autres forces, comme l’ électromagnétisme .
Les nucléons constituent le plus grand pourcentage de la masse d’un atome et déterminent donc la différence entre un élément chimique et l’autre : par exemple, l’atome d’hydrogène n’a qu’un seul proton dans son noyau, tandis que l’atome d’hélium n’a qu’un seul proton dans son noyau. Il a deux protons et un ou deux neutrons, selon l’isotope spécifique.
Numéro atomique
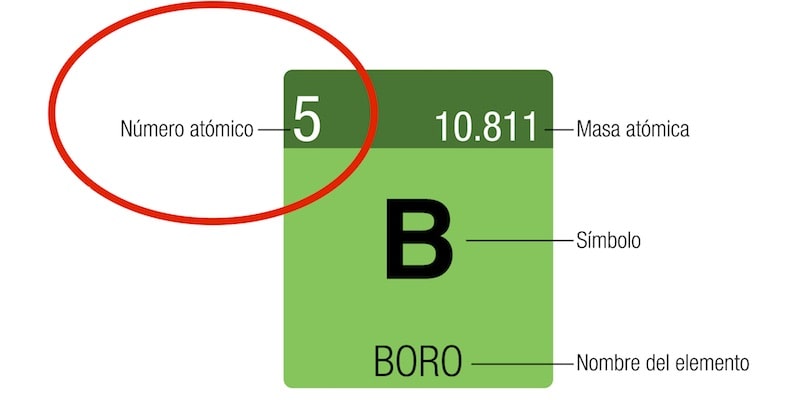
Le numéro atomique (Z) indique combien de protons un type d’atome a dans son noyau. Chaque élément chimique a un numéro atomique différent, bien que son comportement chimique soit plutôt déterminé par le nombre d’électrons qui orbitent autour de son noyau (qui pour un atome neutre est égal au nombre de protons).
Ainsi, par exemple, le chlore (Cl) a 17 protons dans son noyau, de sorte que son numéro atomique est 17. Ce nombre ne varie jamais, pas même entre les isotopes (versions) d’un même atome, puisqu’ils ne diffèrent entre oui que par le nombre de neutrons dans son noyau.
Continuer avec : Antimatière







