Nous expliquons ce qu’est la chaleur et quelles sont les unités de chaleur. Ses différences avec la température, les types de chaleur et des exemples.

Qu’est-ce que la chaleur ?
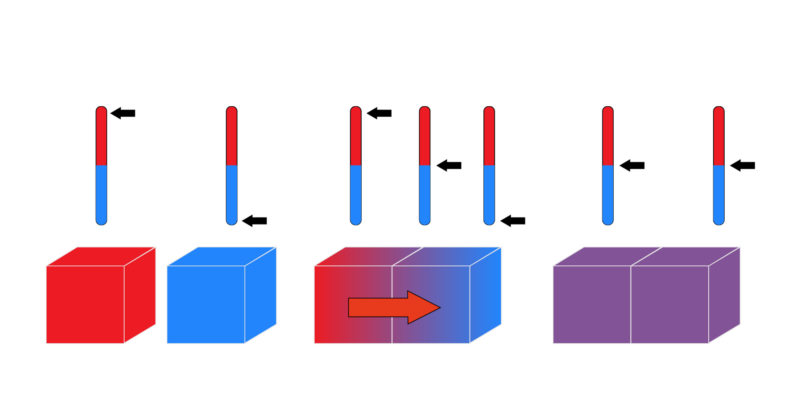
La chaleur est une forme d’énergie qui est transférée spontanément entre différentes zones d’un corps ou d’un corps à un autre.
En thermodynamique , « chaleur » signifie « transfert d’énergie ». Ce transfert a toujours une direction définie par la différence de température entre les corps. La chaleur circule du corps le plus chaud vers le corps le plus froid afin d’atteindre une température d’équilibre.
La chaleur peut être transmise de trois manières différentes :
- Radiation thermique. La chaleur se propage par les ondes électromagnétiques . Tous les corps dégagent ainsi de la chaleur, à moins qu’ils ne soient à une température égale au zéro absolu, 0 Kelvin.
- Conduction thermique. La chaleur est transmise par l’agitation des molécules , ce qui fait augmenter la température, évaporer les liquides , fondre les solides et dilater les corps.
- Convection thermique. La chaleur est transférée par le mouvement d’un fluide , tel qu’un gaz et un liquide. Par exemple, lorsque l’on chauffe de l’eau dans une casserole, la partie qui est en contact avec son fond monte en s’échauffant, tandis que l’eau de surface descend sur les parois en se refroidissant, prenant la place laissée par la partie chaude.
Voir aussi: Conductivité thermique
unités de chauffage
Puisque la chaleur est un transfert d’énergie , elle peut être mesurée comme un gain ou une perte d’énergie. Elle peut donc être mesurée avec la même unité que n’importe quel autre type d’énergie : le joule (qui, en plus de la chaleur, sert à mesurer le travail et l’énergie).
Pour mesurer la chaleur, deux autres unités sont utilisées :
- Calories . Son abréviation est cal et représente la quantité d’énergie nécessaire pour augmenter 1 gramme d’ eau de 1°C.
- Kilocalorie. Il est abrégé kcal et représente l’énergie nécessaire pour élever 1 kilogramme d’eau de 1°C.
Différence entre la chaleur et la température

La chaleur et la température sont des choses différentes, bien qu’elles soient étroitement liées l’une à l’autre. La chaleur est le transfert d’ énergie thermique d’un corps avec une température plus élevée à un autre avec une température plus basse.
La température, quant à elle, est la grandeur physique qui mesure l’état thermique d’un corps et l’ énergie cinétique des molécules qui le composent.
La température, dans le Système international d’unités , peut être mesurée à partir de trois échelles différentes : Kelvin, Celsius et Fahrenheit.
Plus dans: Température
types de chaleur

Différents types de chaleur peuvent être identifiés. Certains d’entre eux sont les suivants :
- Latent. C’est l’énergie nécessaire pour modifier la phase d’un certain volume d’une substance , c’est-à-dire son état (solide, liquide ou gazeux). Lors du changement d’état du solide au liquide, la chaleur latente est appelée chaleur de fusion . Lors du changement d’état du liquide au gaz, la chaleur latente est appelée chaleur de vaporisation . Ces transitions se produisent sans changement de température.
- Sensible. C’est la chaleur qui génère un changement de température du corps qui la perçoit mais qui n’interfère pas avec sa structure moléculaire ni ne produit de changements de phase.
- Séché. Il s’agit d’une méthode thermique de stérilisation qui génère un effet similaire à la cuisson dans les micro -organismes qui composent le corps.
- Spécifique . C’est la quantité de chaleur nécessaire pour augmenter d’un degré la température d’un gramme de masse d’un composé .
- molaire spécifique. C’est la quantité de chaleur nécessaire pour augmenter d’un degré la température d’une mole de masse d’un composé .
Exemples de chaleur
Certaines situations de la vie courante dans lesquelles la chaleur ou le transfert d’énergie est présent peuvent être les suivantes :
- Lors du repassage des vêtements. Après avoir branché l’appareil, il augmente sa température, entre en contact avec le tissu et aide à éliminer les plis.
- Du thé à la tasse. Lorsque du thé chaud est servi dans une tasse, l’eau lui transfère sa chaleur et la tasse augmente sa température (ce que la paume de la main perçoit généralement).
- En servant les aliments dans une assiette. Si l’assiette est en céramique ou en un autre matériau conducteur, les aliments qui y sont servis y conduiront de la chaleur.
- Sable sur la plage. La température rayonnée par le soleil est absorbée par les grains de sable et cette chaleur est transportée, par exemple, jusqu’à la plante des pieds.
- De l’eau au glaçon. Lorsqu’un glaçon est déposé dans un pichet d’eau, l’eau lui transfère sa chaleur par conduction, après quoi le glaçon commence à fondre.
- Lorsque vous faites fondre du chocolat dans votre main. Lorsqu’une personne tient un morceau de chocolat pendant un certain temps, il commence à fondre en raison du transfert de chaleur corporelle.
- En faisant bouillir de l’eau dans une bouilloire. La chaleur de la flamme est conduite à la base de la bouilloire, qui est ensuite transférée à l’eau, portant l’eau à un point d’ébullition .
- Une ampoule allumée. Lorsque l’ampoule est allumée, elle dégage rapidement de la chaleur.